蒲汪旸医生的科普号
- 精选 胃癌临床试验招募(2024年4月更新)
目前我科有多项关于胃癌的临床试验正在入组中(详见下表),想尝试胃癌最新治疗方案的患友可以直接和我联系。联系方式:1.线上联系方式:好大夫上给我留言;2.线下就诊:蒲汪旸医生胃癌专病门诊:苏州大学附属第二医院肿瘤科,每周三下午(三香院区)3.添加微信:
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科762人已读 - 精选 什么是临床试验?如何查找临床试验?
什么是临床试验?临床试验是通过在人体(患者或健康志愿者)进行药物的系统性研究,证实或揭示试验药物在人体的作用、不良反应及试验药物的吸收、分布、代谢和排泄情况。临床试验的最终目的是确定药物本身的疗效与安全性。临床试验是要把我当小白鼠吗?许多病人听说临床试验,可能会想“这是要拿我当试验品?”。实际情况并非如此,临床试验并不是在对新药物毫无了解的情况下盲目开展的。通常在进行临床试验之前,对于新药的疗效、安全性等问题,已经有大量的前期研究,获得充足的信息。药物临床试验通常分为1-3期。1期是给志愿者少量试验药物,仔细监测药物的血液浓度、排泄情况、有益反应和不良作用。随着对试验药物安全性了解的增加,逐渐提高给药剂量,以便确定将来在病人身上使用的合适剂量。2期是初步了解试验药物对疾病的效果和不良反应情况。3期是在对新药治疗效果初步了解的基础上,扩大研究规模,同目前的标准治疗进行对比,进一步确定新药的治疗效果。通常一个药物按次序完成了1、2、3期临床试验,确定疗效和安全性后,才能被批准上市。每个临床试验是保证参加者利益的前提下进行的。有独立的伦理委员会对临床试验的设计方案进行把关,只有在最大限度保障人体试验参加者利益的前提下,伦理委员会才会批准人体临床试验的实施。在参加试验过程中,一旦出现任何意料之外的事件,患者可随时退出和终止研究。临床试验参加者可以从多方面获益。1)正式进入试验后,患者将接受比其他传统治疗更为细致的观察和随访,有权与试验实施医生保持随时沟通。2)多数临床试验都有免费赠药政策,能够提前使用到新药,从中获益。3)有些临床试验有经济补贴。因此,对于现行疗法效果不佳或者经济条件不好,无法承担治疗费用,参加临床试验免费尝试新的治疗方法是一个很好的选择。什么情况下可以参加临床试验?临床试验方案中会明确指出“入选标准”和“排除标准”来确定适合参加这个临床试验的人。“入选标准”规定哪些人适合参加这个临床试验;“排除标准”确定什么样的人不适合这个参加临床试验。符合标准的人都可以参加临床试验。如何获得临床试验的信息?在国内,获取肿瘤药物临床试验信息的途径主要有:一、医院网站或肿瘤科门诊查询;二、登录中国临床试验注册中心网站查询正在进行的药物临床试验信息。网站地址:http://www.chictr.org.cn/index.aspx
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科7002人已读 - 医学科普 化疗副作用之脱发
生了肿瘤,常常需要面对化疗和脱发。不要因为担心脱发,而放弃化疗,把精力放在如何保持健康上。即使脱发,还有很多办法让你保持健康形象。 1. 为什么化疗会导致脱发? 化疗药物杀伤快速生长的肿瘤细胞,同时,也会杀伤体内迅速生长的正常细胞,包括毛囊细胞。 脱发一般从第一次化疗后两周开始。不仅头发会脱落,眉毛、睫毛、阴毛都会不同程度的脱落。可能是大把大把地很快掉光也可能是慢慢脱发。你会发现枕头上、梳子上、衣服上、下水道口有很多毛发。头发是变得稀疏还是全部掉光,取决于化疗药物的种类和剂量。 幸运的是,化疗引起的脱发多数都是暂时的。化疗结束后3~6个月毛发开始再生。新长出来的毛发可能跟你以前的毛发不太一样。比以前卷曲,也不像以前那么黑,不过别着急,当控制毛发颜色的色素细胞功能完全恢复后,你的头发会恢复以前的颜色。 2. 化疗脱发能预防吗? 没有办法能保证化疗不脱发。戴冰帽可以一定程度减少脱发。 冰帽:冰帽或类似的东西能降低头皮温度,减少头皮血流,从而减少头皮部位化疗药物的剂量,减少化疗药物对毛发的影响。化疗过程中使用冰帽,对减少脱发有一定效果。有的患者戴冰帽,会有头痛不适。但头皮肿瘤的患者不适合戴冰帽,因为头皮化疗药物剂量减少,会影响化疗效果。 3. 如何养护头发,应对脱发? 脱发通常是无法预防和控制的。在你治疗过程中采取以下方法,尽可能减轻脱发所致的挫折感和焦虑。 治疗前: 温柔护发:养成爱护毛发的习惯。不要拉直、染色、烫卷发。尽可能让头发自然干,避免用电吹风。现在强健毛发,可能会延迟脱发开始的时间。 考虑剪短发:这会让你感到自己在控制着头发的去留,同时也把处理脱发变得更简单。 准备假发、围巾或帽子等。 治疗过程中: 细心呵护你的头发:治疗期间继续温柔护发,用软齿数字,减少洗头次数,用温和的洗发水。 考虑剃掉剩余的毛发:有些人在掉头发期间会觉得头皮发痒,敏感。剃掉头发,可以减少不适感,减少头发到处掉落的尴尬。 保护头皮:外出时戴帽或围上头巾,保护头皮,防止阳光的曝晒或吹冷空气。 化疗后: 继续温柔护发:新长出来的头发脆弱,容易受到伤害。毛发没有完全恢复健康前不要染发、烫发。染发烫发会损伤新长出来的毛发,刺激敏感的头皮。 耐心:治疗结束后,新的头发会慢慢长出来,新长出来的头发看上去可能没有那么好,但是不要着急,待毛发的损伤完全恢复后,头发就会靓丽如初了。
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科5708人已读 - 典型病例 一例PET-CT改变胃癌治疗方向的病例
老王自觉腹胀,在当地医院胃镜检查发现胃癌,为了评估肿瘤的范围,做了胸腹盆增强CT,CT见胃窦壁增厚,左侧锁骨下淋巴结可见转移可能,第6椎体、胸8、10左侧附件高密度影,转移不除外。胃癌常见的远处转移部位包括肝脏、腹膜,部分患者会出现左侧锁骨上淋巴结转移,腺癌伴左锁骨下淋巴、骨转移发生率不高。有远处转移的胃癌预后比较差,生存期有限,治疗的目标是延长生命。患者家属已经做好姑息性化疗的准备。转机:考虑非常见转移部位,建议完善PET-CT检查。PET-TC结果提示胃窦癌,左锁骨下淋巴结为炎性,骨未见FDG代谢增高。没有远处转移的进展期胃癌,治疗的目标是根治肿瘤。患者家属也松了一口气。患者接受胃癌根治术,术后病理示中分化腺癌,小弯侧淋巴结(0/26)未见癌转移,幽门旁淋巴结(1/5)见癌转移。术后分期II期。PET-CT在肿瘤的诊治中有非常重要的意义,在肿瘤分期、判断治疗效果、判断肿瘤是否残留等方面都有很重要的作用。在这个病例中,相对CT,PET-CT能够更全面的评估肿瘤范围,为制定准确的治疗方案提供更全面的信息。
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科20人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科20人已读 - 胃癌前沿进展 2024 ASCO-GI 胃癌研究进展
新辅助治疗MATTERHORN研究:度伐利尤单抗+FLOT治疗可切除的胃和胃食管交界癌病理完全缓解的地区亚组分析结果研究设计 MATTERHORN研究旨在评估度伐利尤单抗+FLOT治疗可切除的胃和胃食管交界癌的III期临床研究。2023年ESMO会议上报道了中期分析结果。研究共纳入948例患者中,度伐利尤单抗组的pCR率较安慰剂组有显著改善(19%vs7%)。pCR+接近完全病理反应(pnCR)率在度伐利尤单抗组为27%,安慰剂组为14%。今年ASCO-GI上,公布了地区亚组分析结果。所有患者中,180例(19%)来自亚洲。在不同国家的亚组中,观察到与安慰剂联合FLOT相比度伐利尤单抗联合FLOT治疗的pCR均有改善。KEYNOTE-585研究中FLOT队列列第三次中期分析的结果KEYNOTE-585研究评估帕博利珠单抗联合化疗新辅助/辅助治疗局部晚期可切除的胃或胃食管交界处(G/GEJ)腺癌的疗效。研究分为两个队列,主队列评估帕博利珠单抗联合顺铂+卡陪他滨/顺铂+5-Fu,FLOT队列评估帕博利珠单抗+FLOT的疗效。研究设计主要终点:BICR评估的pCR、研究者评估的无事件生存期(EFS)、OS(主队列)、安全性(FLOT队列)2023年ESMO大会上报道了主队列的结果。帕博利珠单抗组pCR率(12.9%vs2%,P<0.00001)明显提高;EFS有延长趋势(44.4vs25.3m;P=0.0198),但统计学差异不显着。此次ASCO-GI会议上报道了FLOT队列结果。FLOT队列共有203名患者,帕博利珠单抗组100名,安慰剂组103名。140人(69%)为淋巴结阳性(N+),79人(39%)基线时患有胃食管腺癌。帕博利珠单抗组和安慰剂组的R0切除率分别为79%和80%。CR率分布为17.0%(95%CI,10.2-25.8)和6.8%(95%CI,2.8~13.5)。帕博利珠单抗组中位EFS未达到,安慰剂组为30.9个月。两组患者均未达到中位OS,两组患者24个月的OS率分别为72%和73%。MATTERHORN和KEYNOT-585都是关于免疫联合化疗应用于胃癌围手术期治疗的III期临床研究。两个研究入组的都是T≥3或N+性的患者。研究结果上看,杜伐利尤单抗/帕博利珠单抗联合FLOT方案的pCR率非常接近,期待EFS和PD-L1表达亚组的结果。晚期一线比较多西他赛-奥沙利铂-卡培他滨/5-氟尿嘧啶(DOC/F)然后多西他赛维持与CAPOX/mFOLFOX-7治疗晚期胃癌的疗效随机开放标签前瞻性III期临床研究(DOC-GC研究)研究设计主要终点:OS;次要终点包括无进展生存率和不良事件发生率结果:在2020年7月至2022年11月期间入组的324名患者中,305名患者可进行评估分析(A组:156例;B组:149例)。A组和B组的中位OS分别为10.1个月(95%:9.2-10.9)和8.9个月(95%可信区间:7.3-10.5),差异无统计学意义[p=0.70]。两组中位PFS差异无统计学意义[A组:7.1个月(95%CI:6.1-8.1);B组:6.2个月(95%CI:5.7-6.8);P=0.39]。B组患者出现3/4级中性粒细胞减少症的比例高于A组(21%比5.1%;p<0.001),其他与治疗相关的副作用在两组患者中相似。与B组相比,A组患者倾向于接受二线治疗的比例更大(38%比26%;p=0.07)。晚期胃癌一线的化疗方案是选择两药,还是三药,争论由来已久。三药方案DCF虽然在III期研究中达到了研究终点,但不良反应亦有明显增加,限制了它的临床运用。JCOG1013研究显示在CS的基础上加上多西他赛(DCS方案)并未改善生存期。此次会议报告的DOC-GC研究也显示由5-氟尿嘧啶/卡培他滨和奥沙利铂组成的双重方案中增加多西紫杉醇并不能改善晚期GEJ/G癌症患者的生存。JCOG1013和DOC-GC研究探索增加一个药物的疗效,可能考虑到不良反应,对其他两药的剂量强度也进行了变更。其次,后线的治疗可能会影响OS的结果。晚期后线NIVOFGFR2研究:纳武利尤单抗联合CapeOX对既往未经治疗的FGFR2阳性、PD-L1阳性晚期胃癌患者的疗效和安全性:单臂、多中心、2期研究方法:入组初治、转移性、HER2阴性、PD-L1CPS≥5(DAKO28-8)、FGFR2 2+或3+(AbcamEPR24075-418)胃腺癌患者。患者接受纳武利尤单抗联合CapeOX治疗。主要终点是1年PFS率。结果纳入23名患者,78%患者有≥2个转移灶;CPS(5-9)22%,(≥10)78%。1年PFS率为30.4%。中位PFS为6.2个月(95%CI4.4-7.6)。ORR为21.7%,其中有1例完全应答。数据截止时的中位随访时间为11.8个月,未达到中位OS。9例(39.1%)患者出现了3级治疗相关不良反应。纳武利尤单抗联合化疗已被批准用于PD-L1阳性转移性胃癌的一线治疗。FGFR2在30%的胃癌患者中过表达。FIGHT研究显示bemarituzumab+mFOLFOX6一线治疗FGFR2阳性的不可切除胃癌的能够延长PFS,客观缓解率为57.9%。对于PD-L1CPS≥5同时FGFR2阳性患者是选择免疫联合化疗还是bemarituzumab联合化疗?NIVOFGFR2研究中期分析表明,nivolumabin与化疗联合治疗FGFR2阳性、PD-L1阳性转移性GC患者疗效一般,安全性可接受。德曲妥珠单抗作为新辅助治疗HER2阳性胃癌和胃食管交界腺癌的II期研究(EPOC2003)。方法纳入符合条件的患者为临床分期为T2-4和/或N+、无远处转移、既往未经治疗的局部进展期胃癌或胃食管结合部腺癌。研究包括主队列和探索性队列。主要队列是HER2阳性的患者,定义为IHC3+或IHC2+,局部评估为ISH+。探索性队列是HER2低表达(IHC1+或2+,ISH阴性)且血清HER2-ECD超过11.6ng/ml的患者。术前德曲妥珠单抗治疗3个周期,然后手术。主要终点是中央评估的主要病理反应(MPR)率,预期为45%,无效阈值为20%。主队列的计划样本量为27例,单侧α为10%,功率为90%,另外10例纳入探索性队列。结果2021年11月至2022年11月,27名患者被纳入主队列。大多数患者的IHC3+(24人)。临床分期从II/III/IVa分别为2/21/4例。其中,26人完成了计划的3个疗程的T-DXd,1人因毒性中止治疗。25名患者完成了R0切除术,1名患者进行了R1切除术。MPR率为14.8%,未超过预定的20%。pCR率为3.7%。结论在这项2期研究中,德曲妥珠单抗对晚期HER2阳性胃癌或胃食管腺癌具有适度的单药活性。计划在围手术期将T-DXd与卡培他滨和durvalumab联合使用,以评估是否能提高疗效和预后。输注氟尿嘧啶和每周多西他赛一线治疗骨髓转移(BMM)和弥散性血管内凝血(DIC)胃癌的多中心II期试验方法:这是一项单臂试验。采用西蒙两阶段优化设计。符合条件的病例包括年龄18-75岁,组织学确诊为胃癌,已有BMM,明显DIC,血小板≤50109/L,ECOG评分≤3。氟尿嘧啶200mg/㎡,d1-21;多西他赛25mg/㎡,d1、8、15,q4w。血液学反应(HeR)的定义是血小板恢复到正常范围。主要终点为HeR率。次要终点是达到HeR的时间(TTHeR)、一个月死亡率(OMM)、OS、不良事件(AE)和生活质量(QoL)。结果:2021年1月至2022年9月,来自中国三个中心的24例HAGC病例入选(详见下表)。共完成20例HeR,HeR率为83.3%。中位TTHeR为13天,OMM为12.5%。中位OS为242天。7名患者(29.2%)发生了3级不良反应,其中最常见的是口腔炎(4例,16.7%)和转氨酶升高(3例,12.5%)。治疗期间和治疗后的生活质量均有明显改善。伴有骨髓转移和弥散性血管内凝血的胃癌预后很差。由于血小板减少,这类患者能否从细胞毒性药物治疗中获益不清楚。本研究中氟尿嘧啶+多西他赛方案耐受性良好,在1线治疗中显示出良好的疗效。胃癌伴巨大淋巴结转移的新辅助化疗后预防性主动脉旁淋巴结清扫术在日本,广泛淋巴结转移包括沿腹腔动脉及其分支的巨大淋巴结转移(巨大N2)和主动脉旁淋巴结转移(PAN)。新辅助化疗(Noadjuvantchemotherapy,NAC)后进行D2胃切除术和主动脉旁淋巴结清扫术(PAND)是广泛淋巴结转移(ELM)胃癌的标准治疗。然而,PAND对有BulkyN2但无PAN受累的胃癌的益处尚不清楚。本研究旨在评估NAC后预防性PAND对这部分患者的疗效。方法回顾性研究了2008年至2019年期间因BulkyN2(+)但PAN(-)胃癌接受新辅助化疗后进行R0胃切除术的21例患者。肿大淋巴结的定义为一个淋巴结3厘米或两个相邻淋巴结各1.5厘米。患者分为两组:D2+PAND组(11例)和D2组(10例)。我们比较了两组患者的临床病理特征、复发模式和生存结果。结果:与D2组相比,D2+PAND组的手术时间更长(p=0.006),组织学类型倾向于未分化(p=0.063),病理反应更好(p=0.086),辅助化疗率更高(p=0.090)。两组患者的yp分期相似。D2+PAND组有两名患者(18%)发现病理PAN转移。D2组有7例(70%)患者复发,D2+PAND组有3例(27%)患者复发。两组复发患者中,分别有4例(40%)和1例(10%)患者出现淋巴结复发。D2+PAND组的总生存期、无复发生存期和疾病特异性生存期明显优于D2组(P分别为0.008、0.008和0.020)。结论NAC后预防性PAND可降低BulkyN2但未累及PAN的局部晚期胃癌的复发风险。特瑞普利单抗联合CAPOX新辅助治疗dMMR/MSI-H局部进展期胃癌或食管胃交界腺癌的临床研究:NICEII期试验C组的结果。方法:NICE试验是一项多中心、多队列II期试验,队列C评估特瑞普利单抗联合CapeOX方案作为围手术期治疗dMMR/MSI-H的局部GC或EGJC的安全性和有效性。纳入影像学和腹腔镜分期cT3-4aNxM0或cT2N+M0患者。患者(pts)在手术前后接受了特瑞普利单抗240mg联合标准剂量CapeOX方案。主要终点是主要病理反应率。结果:14名患者术前完成了全部4个周期的治疗,1名患者因AEs完成了2个周期的治疗。无一人出现疾病进展,1名患者在放射学和内镜检查中获得完全临床反应并拒绝手术,其他14名患者均接受手术治疗,R0切除率为100%(14/14)。pCR率为78.6%(11/14)。5例患者(15例)发生了与治疗相关的3/4级AE。一名患者在两个周期治疗后出现了3级免疫相关肝毒性,在接受类固醇治疗后痊愈。没有患者在围手术期死亡,一名患者在术后238天死于COVID-19,且未复发。所有患者均未发现疾病复发。mIHC显示,达到pCR的患者治疗后肿瘤区域内的CD20+B细胞、CD3+T细胞、NKdim细胞和M1巨噬细胞明显减少。目前,dMMR/MSI-H是公认的胃癌免疫治疗疗效预测标志物。Keynote-059、Keynote-061和Keynote-062研究中的MSI-H胃癌患者,帕博利珠单抗的ORR分别未为57.1%,46.7%和57.1%,Keynote-062研究中帕博利珠单抗加化疗的ORR为64.7%,单纯化疗的ORR为36.8%。2023年ESMO公布的NOLIMIT研究的初步结果显示纳武利尤单抗加低剂量伊匹单抗一线治疗进展期胃或食道胃交界处MSI-H腺癌患者ORR为62.1%(95%CI:42.3-79.3),中位PFS为13.8。卡瑞利珠单抗联合阿帕替尼和SOX一线治疗产甲胎蛋白胃或胃食管交界处腺癌患者:一项单臂、多中心、II期试验方法:纳入初治不可切除/复发或转移性G/GEJ腺癌、血清AFP>2ÍULN或IHC染色法AFP阳性。患者接受4个周期的标准S-1加奥沙利铂和卡瑞利珠单抗加阿帕替尼(250毫克,每天1次)治疗。随后卡瑞珠单抗加阿帕替尼治疗达24个月或疾病进展或不可接受的毒性反应。主要终点是ORR。结果:共有36名患者入组并接受治疗。35例患者可评估肿瘤反应。中位年龄为63岁,其中30名患者为男性。94.5%的患者为IV期。血清AFP水平中位数为739.8ng/ml。疗效在FAS群体(n=36)中进行了评估。2例完全应答(CR,全部确认),22例部分应答(PR,18例确认),7例病情稳定(SD)。因此,未经证实的ORR为66.7%(24/36),DCR为86.1%(31/36),证实的ORR为55.6%(20/36)。中位PFS和OS尚不成熟。13名患者(36.1%)发生了3级不良事件。最常见的3级TRAE是中性粒细胞计数下降(13.9%)、高血压(8.3%)和腹泻(5.6%)。结论在既往未接受过系统治疗的AFP生成型G/GEJ腺癌患者中,卡瑞利珠单抗联合阿帕替尼与SOX联合治疗后,再用卡瑞利珠单抗联合阿帕替尼治疗,显示出良好的抗肿瘤活性和可接受的安全性。
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科8人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科8人已读 - 典型病例 一例以胃出血、胃潴留为首发症状胃癌患者的药物治疗
患者是78岁的老年男性,平时生活自理,打牌、烧饭。一日,家人为其清洗衣裤时,发现黑便,其后呕吐咖啡渣样物,立即送至我院。在急诊查CT检查见胃窦壁增厚。遂行胃镜检查胃内情况。第一次胃镜检查,食管和胃腔见大量宿食潴留,无法观察。放置鼻胃管,洗胃、胃肠减压后再次胃镜看到了肿瘤的形态和位置:胃体、胃角、胃窦多发溃疡深浅,胃体下部至胃角、胃窦小弯侧弥漫性粘膜肿胀,可见较深溃疡,底覆污苔,反复冲洗,可见可疑血管头。胃镜病理提示腺癌。患者胃癌诊断明确,能否手术治疗?腹盆腔增强CT见提示胃角胃窦壁增厚;肝胃间隙、腹膜后腔及腹腔内多发增大淋巴结,考虑转移。患者肿瘤范围较广,手术无法根治,遂来到肿瘤科。患者胃管中一直有咖啡色液体引流出来,提示胃出血还没有停止。患者高龄,胃癌晚期,合并胃出血、胃潴留,营养不良,急需有效的治疗控制肿瘤,缓解症状,减轻痛苦。给予信迪利单抗+FLOT方案治疗后第3天,胃管引流液体转为淡黄色,并且引流量逐渐减少。治疗后10天,患者饥饿感明显,吵着要吃东西。拔除胃管,患者进食半流质,未再出现呕吐。随着新药,胃癌药物治疗的效果有了显著提高。FLOT是目前客观有效率最高的化疗方案,化疗基础上联合PD-1单抗,能进一步提高效果。患者以胃出血、胃潴留为首发病症,需要尽快控制病情,缓解出血、梗阻症状,纠正营养不良状态。虽然3药方案不良反应较大,在适当减量基础上,密切观察,取得了非常好的近期疗效。
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科16人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科16人已读 - 胃癌前沿进展 2023 ESMO 胃癌治疗进展
2023年ESMO年会于10月20日-10月24日在西班牙马德里召开。下面就本次会上胃癌治疗相关研究进展做一梳理。新辅助免疫+化疗是近几年胃癌新辅治疗研究的热点,已有多个II期临床研究结果显示免疫+化疗新辅助治疗胃癌有较高的病理完全缓解率(pCR)和主要病理缓解率(MPR)。今年ESMO上报道了MATTERHORN研究、KEYNOTE-585研究和DragonIV3项关于免疫联合化疗新辅助治疗胃癌的III期研究的结果。MATTERHORN研究中期结果:度伐利尤单抗+FLOT治疗可切除的胃和胃食管交界癌的III期临床研究研究设计结果:474名患者随机分配到每个治疗组。两组基线特征平衡。患者中,胃癌比例68%、cT3:66%;cT4,25%;cLN+:70%。度伐利尤单抗组的pCR率较安慰剂组有显著改善(19%vs7%);pCR+接近完全病理反应(pnCR)率在度伐利尤单抗组为27%,在安慰剂组为14%。度伐利尤单抗组的手术率和R0切除率(分别为87%和86%)与安慰剂组(分别为84%和86%)相似。两组之间的不良事件发生率相似。在围手术期FLOT治疗中添加度伐利尤单抗可以提高pCR率。无事件生存(EFS)情况待后续随访结果。KEYNOTE-585研究KEYNOTE-585研究是评估帕博利珠单抗联合化疗新辅助/辅助治疗局部晚期,可切除的胃或胃食管交界处(G/GEJ)癌症疗效的III期临床研究。研究分为两个队列,主队列评估帕博利珠单抗联合顺铂+卡陪他滨/顺铂+5-Fu,FLOT队列评估帕博利珠单抗+FLOT新辅助治疗进展期胃癌的疗效。此次会议报道了主队列第三次中期分析的结果。研究设计主要研究终点:BICR评估的pCR、研究者评估的EFS、OS(主队列)、安全性(FLOT队列)结果:两队列共纳入1007名患者,主队列中帕博利珠单抗组和安慰剂组各402名患者。FLOT队列帕博利珠单抗组100名,安慰剂组103名患者。主队列中,与安慰剂组相比,帕博利珠单抗组的pCR率(12.9%vs2%,P<0.00001)明显提高;EFS有延长趋势(44.4vs25.3m;P=0.0198),但统计学差异不显着。两组中位OS分别为60.7vs58.0m(HR0.90;95%CI,0.73-1.12)。由于EFS的改善无统计学意义,研究没有正式评估OS主要终点。EFS亚组分析主队列组的OSDragonIV研究中期分析:卡瑞利珠联合阿帕替尼和化疗治疗局部晚期可切除胃或胃食道交界部(G/GEJ)腺癌的III临床研究研究设计结果:SOX+阿帕替尼+卡瑞利珠组和SOX组各入组180例患者。两组患者的新辅助完成率为分别为91.1%vs.93.9%;手术完成率为86.1%vs.86.7%。SOX+阿帕替尼+卡瑞利珠组与SOX组相比,pCR率提高了13.7%(95%CI7.2-20.1,p<0.0001),两组的pCR率分别为18.3%(95%CI13.0-24.8)和5.0%(95%CI2.3-9.3);两组患者MPR率为51.1%和37.8%。整个治疗期间,SOX+阿帕替尼+卡瑞利珠组与SOX组对比,≥10%的治疗相关不良事件(TRAEs)包括中性粒细胞减少、白细胞计数降低和血小板减少等,其中≥3级以上TRAEs包括:中性粒细胞减少(19%vs.10.1%),白细胞计数降低(8.4%vs3.9%)、血小板减少(11.7%vs.10.7%)、体重减轻(5.6%vs.2.8%)、高血压(5.6%vs.0)、γ-谷氨酰转移酶升高(6.7%vs.0)等。SOX+阿帕替尼+卡瑞利珠与单纯化疗相比明显提高pCR率,期待EFS的结果。RESOLVE研究结果更新RESOLVE研究是比较奥沙利铂联合S-1(SOX)的围手术期化疗与SOX或奥沙利铂联合卡培他滨(XELOX)的术后化疗治疗局部进展期胃腺癌疗效的III期临床研究。2019年的ESMO大会上报告了研究结果,与术后XELOX方案辅助化疗(B组)相比,围手术期SOX方案化疗(C组)提高了3年无病生存率(59.4%)。术后SOX(A组)3年DFS率为56.5%,不劣于术后XELOX(51.1%)。今年ESMO大会上,张小田教授公布了RESOLVE研究5年生存结果。研究设计主要研究终点3年DFS,次要研究终点5年总体生存率和安全性结果:SOX围手术期治疗与CapOx相比改善患者5年OS%(60.0%vs52.1%;HR0.79,95%CI[0.62-1.00],p=0.049),SOX围手术期治疗较CapOx显著降低21%的死亡风险;SOX术后辅助治疗非劣于CapOx(61.0%vs52.1%;HR0.77,95%CI[0.61-0.98],p=0.033)。SOX围手术期治疗与CapOx相比显著改善患者5年DFS%(53.2%vs45.8%;HR0.79,95%CI[0.63-0.98];p=0.034)。晚期一线Keynote-811:帕博利珠单抗联合曲妥珠单抗和化疗治疗Her-2阳性转移性胃或胃食道交界部腺癌的III临床研究研究设计研究主要终点:PFS和OS;关键次要终点:ORR和DOR结果:共纳入698例患者,帕博利珠单抗组350例,对照组348例,两组的PFS分别是10.0和8.1m;HR0.72;95%CI0.60~0.87;p=0.0002)。在PD-L1CPS≥1患者中,两组的中位PFS分别为10.8mo和7.2mo(HR0.70;95%CI,0.58~0.85)。OS仍在随访中。目前两组的OS分别为20和16.8m。帕博利珠单抗组和对照组的ORR分别为73%和58%,在PD-L1CPS≥1的患者中,ORR分别为73.2%和58.4%。中位缓解持续时间(DOR)分别为11.2个月和9.0个月。大约31%和19%的应答者的应答持续时间≥24个月。Her-2阳性晚期胃癌帕博利珠单抗+曲妥珠单抗+化疗明显提高客观有效率,延长PFS。NOLIMIT研究的初步结果(WJOG13320G/CA209-7W7):纳武利尤单抗加低剂量伊匹单抗一线治疗进展期胃或食道胃交界处MSI-H腺癌患者的II期研究研究设计:纳入MSI-H、不能切除的晚期、复发或转移性、初治胃腺癌患者,给予纳武利尤单抗240mgq2w,伊匹单抗1mg/kgq6w,直至病情进展或出现不可接受的毒性。主要终点为客观有效率(ORR)。结果:2020年11月至2022年8月,从935例筛查病例中纳入29例患者。中位年龄为75岁(54-84岁),其中44.8%为男性。ORR为62.1%(95%CI:42.3-79.3),其中3名患者(10%)完全缓解。DCR为79.3%(95%CI,60.3~92.0)。中位PFS为13.8(95%可信区间,13.7-NR)个月,中位DOR和OS尚未达到。停止治疗的最常见原因是不良事件。安全性与已知的nivolumab加小剂量ipilimumab的不良反应一致。结论:在MSI-HGC患者中,联合应用nivolumab和小剂量ipilimumab的非化疗策略显示出高而稳健的疗效和良好的耐受性。RATIONALE-305研究结果更新RATIONAL-305是评估铂/氟嘧啶联合替雷利珠单抗一线治疗局部晚期或转移性胃/胃食管结合部腺癌患者的安全性和有效性的III期临床研究。2023年ASCO-GI上报道了研究结果,与安慰剂相比,替雷利珠单抗能够明显延长患者中位OS(17.2mvs12.6m)。替雷利珠单抗与安慰剂组的PFS分别胃7.2vs5.9个月;ORR分别为50.4%vs43.0%。本次会议上公布了RATIONALE-305试验的最终分析结果。研究设计结果:997名患者被随机分配至试验组(n=501)或安慰剂组(n=496)。与ITT人群中安慰剂组相比,试验组的OS显著改善,两组中位OS分别为15.0个月和12.9个月。其它主要疗效结果见下表:GLOW研究数据更新GLOW研究是评估Zolbetuximab联合CAPOX用于治疗Claudin18.2阳性胃或食管胃结合部腺癌的随机对照III期研究。2023年ASCO大会上报道了GLOW研究的结果,Zolbetuximab组对比安慰剂组延长了PFS(8.21vs6.8m,P=0.0007)和OS(14.39vs12.16m,P=0.0118)。试验组和对照组的ORR分别为42.5%VS40.3%。本次ESMO会议上更新了疗效和安全性数据。研究设计结果:在数据截止点(2023年6月29日),507名患者被分配到Zolbetuximab+CAPOX(n=254)或PBO+CAPOX(n=253)。zolbetuximab组与安慰剂组的中位PFS分别为8.3和6.8个月(HR0.68[95%CI0.55,0.85])。Zolbetuximab组和安慰剂组中位OS分别为14.3和12.2个月(HR0.77[95%CI0.62,0.95]);24个月OS发生率为28.3%对18.8%.对可测量病灶的患者中进行事后分析,Zolbetuximab组和安慰剂组的ORR分别为54.1%vs48.5%。Zolbetuximab组最常见的治疗相关不良反应是恶心(Zolbetuximab组:68.9%vsPBO组:50.2%)、呕吐(66.1%vs31.3%)和食欲下降(41.3%vs34.5%);两组之间严重不良反应发生率相似(48.0%对50.6%)。Spotlight研究结果更新Spotlight是评估佐妥昔单抗+mFOLFOX6一线治疗CLDN18.2+/HER2-局部晚期无法切除或转移性胃或胃食道交界处腺癌的3期研究,今年ASCO-GI上公布了研究结果结果,与安慰剂相比,佐妥昔单抗+mFOLFOX6显著改善PFS(10.61vs8.67个月)和OS(18.23vs15.54个月)。两组ORR分别为53.8%vs48.8%。此次会议更新了疗效和安全性数据。研究设计结果:在数据截止日期(2023年6月29日),佐妥昔单抗组(n=283)与安慰剂组(n=282)的中位PFS分别为11.0vs8.9个月(HR0.73[95%CI0.59,0.91],P=0.0022);中位OS为18.2vs15.6个月(HR0.78[95%CI0.64,0.95],P=0.0067);独立评审委员会评估的ORR分别为61.1%vs62.4%。恶心、呕吐、食欲减退是Zolbetuximab联合mFOLFOX6最常见的治疗相关不良事件,这与GOLOW研究(Zolbetuximab联合CAPOX)最新的分析结果一致。晚期二线及以后RINDBeRG试验:雷莫西尤单抗联合伊立替康对比伊立替康三线或后线治疗雷莫西尤单抗治疗过的晚期胃癌的III期临床研究研究设计主要终点是总生存期结果:共纳入402名患者,雷莫西尤单抗组202名,伊立替康组200名。两组的中位OS分别为9.4个月和8.5个月(校正HR0.909,95%置信区间0.738-1.119;p=0.369)。中位PFS分别为3.8个月和2.8个月(HR0.722,95%CI0.590-0.884;p=0.001),ORR分别为22.1%(33/149)和15.0%(25/167)。雷莫西尤单抗耐药后,在伊立替康中加入雷莫西尤单抗可改善PFS和ORR,毒性可控,但未达到OS的主要终点。Infigratinib治疗FGFR2基因扩增的局部进展期或转移性胃癌或胃-食管交界腺癌患者的疗效和安全性FIGHT研究结果显示评价贝马妥珠单抗(bema)联合mFOLFOX6一线治疗FGFR2b+晚期胃/胃食管交界处腺癌与单纯化疗相比,显著改善无进展生存期(中位PFS:9.5个月vs7.4个月;HR=0.68)和总缓解率(ORR:46.8%vs33.3%)。Infigratinib是一种口服的、ATP竞争性的成纤维细胞生长因子受体酪氨酸激酶抑制剂(TKI),靶向纤维细胞生长因子受体(FGFR)蛋白,阻断下游活性。LB1001-201试验(NCT05019794)队列1评估infigratinib在既往二线或以上系统治疗失败的、伴有FGFR2基因扩增(FISH检测)的局部进展期或转移性胃癌或胃食管结合部腺癌的疗效和安全性。ORR为25.0%,DCR为80.0%,mDOR为3.8个月,mPFS3.3m,mOS8.0m。15/19例肿瘤缩小,最大缩小幅度达78.5%。≥三级TRAE占42.9%。
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科20人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科20人已读 - 入组中的胃癌临床试验 赛沃替尼治疗MET扩增胃癌患者的II期临床试验
目前苏州大学附属第二医院肿瘤科正在开展一项“赛沃替尼治疗MET扩增胃癌患者的II期临床试验”。赛沃替尼是一种强效、高选择性的口服小分子间质上皮转化因子(MET,一种受体酪氨酸激酶)抑制剂,用于治疗MET扩增的晚期或转移性胃癌或胃食管结合部患者。MET驱动的胃癌预后一般较差,对化疗不敏感。既往研究提示,伴有MET扩增的患者接受赛沃替尼单药治疗,客观有效率达50%。主要入组患者:不能手术或转移性胃癌患者。联系方式如果您对本研究感兴趣,想了解更多相关信息,可以直接与我联系。1.线上联系:好大夫上给我留言2.线下就诊:蒲汪旸医生胃癌专病门诊:苏州大学附属第二医院肿瘤科,每周三下午(三香院区)3.扫描下方二维码,关注我的公众号,公众号上给我留言
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科16人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科16人已读 - 胃癌前沿进展 2023 ASCO 胃癌研究进展
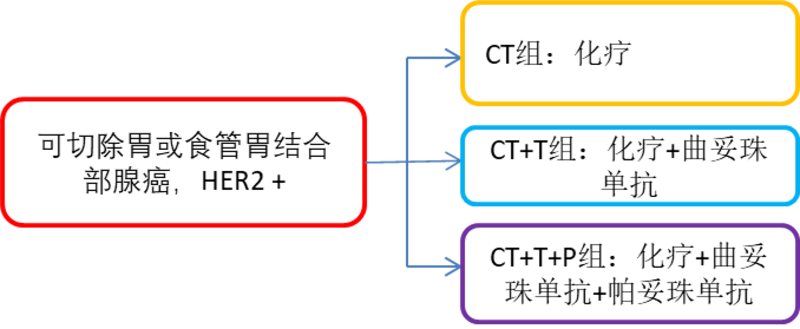
2023年ASCO会议在美国芝加哥召开,本次会议的主题为:“与患者合作:癌症治疗与研究的基石(PartneringWithPatients:TheCornerstoneofCancerCareandResearch)”。会议上,胃癌领域共有三十余项摘要,令我关注的研究包括特瑞普利单抗联合SOX或XELOX围手术期治疗,辅助免疫治疗的ATTRACTION5研究以及EPCAMCAR-T、端粒酶(OBP-301)联合帕博利珠单抗治疗晚期胃癌的研究。新辅助Poster 4057 EORTC1203INNOVATION研究:评估在HER-2阳性胃和食管胃交界部癌症围手术期化疗中加入曲妥珠单抗(含或不含帕妥珠单抗)疗效的II期临床研究研究设计方法:研究计划入组215名患者,由于入组缓慢,患者招募提前终止。共161名患者符合纳入标准并以1:2:2的比例随机分配到:单独化疗(CT)组(35名)、CT+曲妥珠单抗(T)组(67名)和CT+T+帕妥珠单抗(P)组(70名患者)。化疗方案最初为顺铂+卡培他滨,术前和术后3个周期。FLOT-4研究发表后,化疗方案改为四个周期FLOT,FOLFOX或CAPOX作为不符合FLOT条件患者的替代方案。该研究设计为具有80%的能力检测mpRR从CT的25%增加到CT+T+P或CT+T的45%,单侧α为10%。首先对CT+T+P与CT进行比较,如果阳性,则将CT与CT+T进行对比。结果:与单纯化疗相比,化疗+T+P主要病理缓解率增加3.1%(80%CI:[-9.5%,15.7%],单侧p=0.378),无统计学意义;化疗+T组的mpRR增加了13.7%(80%置信区间:[0.7%,26.7%],单侧p=0.099)。基于化疗方案进行分层分析,化疗方案修改为FLOT后,CT,CT+T,CT+T+P三组的mpRR分别为33.3%、53.3%和37.9%,而修改前分别为8.3%、16.7%和12.5%。对于HER2阳性转移性胃癌,曲妥珠单抗+化疗与单纯化疗相比,能够延长生存,提高客观有效率(47%VS35%)。有II期临床研究,评估曲妥珠单抗联合FLOT(HER-FLOT研究)或联合XELOX(NEOHX)新辅助治疗可切除胃或食管胃结合部腺癌的疗效,显示联合治疗可以提高客观有效率和病理缓解率。虽然在HER2阳性乳腺癌中,帕妥珠单抗的加入可改善生存。但在在HER2阳性晚期胃癌加入帕妥珠单抗不能改善患者的生存(JACOB研究)。从EORTC1203INNOVATION研究结果看到,CT+T+P联合治疗与单纯化疗相比没有明显提高主要病理缓解率。然而,化疗+曲妥珠单抗与单纯化疗相比,有比较高的主要病理缓解率,尤其是以FLOT作为化疗方案。Poster4001 特瑞普利单抗(toripalimab)联合SOX或XELOX与单独应用SOX或XELOX治疗局部进展期胃或胃食道交界部癌症的前瞻性、随机、开放标签II期试验研究设计结果:2019年10月至2022年6月,共纳入108名患者(特瑞普利+化疗组,n=54;化疗组,n=54)。几乎所有患者都在诊断时进行了腹腔镜探查,基线特征见下图。特瑞普利单抗联合化疗组患者的TRG0/1比例高于化疗组(44.4%vs20.4%;P=0.009),pCR率也更高(24.1%vs9.3%;P=0.039)。特瑞普利+化疗组的降期比例高于单纯化疗组(ypT0-2:46.3%比22.2%[P=0.002];ypN0-1:38.9%比16.7%[P=0.024])。手术并发症发生率(特瑞普利+化疗组为11.8%,化疗组为13.5%)和死亡率(1.9%比0%)以及治疗相关的3-4级不良事件(27.8%比25.9%)在两组之间相当。结论:围手术期特瑞普利单抗联合化疗提高病理缓解率,可能是局部晚期可切除胃癌或GEJ癌患者的有希望的治疗选择。辅助Poster 4065 JACCROGC-07五年随访结果背景:JACCROGC-07是一项随机对照试验,旨在探讨D2切除术后pStageIII期胃癌术后S-1/多西紫杉醇辅助治疗的疗效。将pStageIIIGC患者随机分为接受S-1/多西他赛或S-1单药治疗组。根据分期(IIIA、IIIB、IIIC)和组织学类型(分化或未分化)进行分层。主要终点为3年无复发生存(RFS),次要终点为OS、TTF和安全性。第二次中期分析表明,与单独使用S-1相比,S-1/多西他赛可显著改善RFS。此次会议上报道了5年随访数据。结果:在915名随机分配的患者中,912名患者被纳入意向治疗(ITT)分析。最终分析显示,在63.72个月(3.52-111.87)的中位随访期内,ITT人群中确诊426例复发和373例死亡。S-1/多西他赛组5年RFS 59.8%显著优于S-1组的50.6%(HR0.726,95%CI:0.599-0.879,p=0.0010),S-1/多西他赛组和S-1组的5年OS分别为67.9%和60.3%(HR0.752,95%CI:0.613-0.922,p=0.0059),证实了对患者生存的显著改善作用。结论:对于接受D2胃切除术而未进行新辅助化疗的pIII期胃癌患者,应考虑使用S-1联合多西紫杉醇进行辅助治疗。Oral 4000 ATTRACTION-5:纳武利尤单抗联合化疗用于pStageIII期胃或胃食道交界处(G/GEJ)癌术后辅助治疗的III期研究研究设计结果:2017年2月至2019年8月,共有755名患者接受了随机分组。14%患者肿瘤细胞PD-L1表达(TPS)>1%,82%的患者TPS<1%。纳武利尤单抗+化疗组(N+C)的3年RFS率为68.4%(95%CI,63.0-73.2),安慰剂+化疗组(P+C)为65.3%(95%CI,59.9-70.2),未达到中心评估RFS的主要疗效终点(HR,0.90;95.72%CI,0.69-1.18;P=0.4363)。亚组分析显示TPS>1%的患者中,N+C与P+C相比,能提高3年RFS(HR0.33;95%CI0.14-0.75)。 计划的术后辅助治疗完成率在N+C组为61.5%,在P+C组为71.4%。N+C组3级TRAEs,严重TRAEs和导致停药的TRAEs发生率分别为54.4%,25.3%和9.2%,P+C组分别为46.8%,10.7%和3.5%。ATTRACTION-5研究结果显示D2或更大范围胃切除术后pStageIIIG/GEJ癌症患者纳武利尤单抗+化疗与单纯化疗相比没有明显提高RFS。亚组分析结果看到,IIIC期患者、TPS>1%患者,纳武利尤单抗+化疗与单纯化疗相比能够提高3年RFS率。从Checkmate-649研究结果看,纳武利尤单抗+化疗能延长CPS>5%患者的OS。从既往研究结果看,TPS<1%的患者中,有60-80%的患者是CPS阳性的,期待TPS阴性而CPS阳性患者以及MSI患者亚组分析的结果。晚期一线Poster 4014 KEYNOTE-859研究中基于PD-L1水平分层分析的结果。今年ESMOVirtualPlenary会议上首次公布Keynote-859的研究数据。KEYNOTE-859研究评估了HER2阴性晚期G/GEJ癌帕博利珠单抗+化疗(FP/CAPOX)用于HER-2阴性晚期胃癌/胃食管连接部腺癌一线治疗的疗效和安全性。ITT人群中,帕博利珠单抗+化疗与单纯化疗相比,显著改善OS(HR0.78,95%CI0.70-0.87;P,0.0001)、PFS(HR0.66,95%CI0.67-0.85;P,00001)和ORR(51.3%vs42.0%;P=0.000009)。今年ASCO会议上,研究者介绍了PD-L1联合阳性评分(CPS)>1和CPS>10人群的疗效结果。研究设计结果:基线特征在治疗组和人群之间大体一致。在PD-L1CPS≥1和≥10人群中,在FP或CAPOX中添加帕博利珠单抗可显著改善OS、PFS和ORR。详细结果见下表。Poster 4045 随机2期IKF-S628/AIO-STO-0417(Moonlight)试验中FLOT+纳武利尤单抗队列结果Moonlight研究是一项多队列II期试验。在2022年ESMO会议上报道了A1组(FOLFOX+nivo+ipi)和序贯治疗的A2组(mFOLFOX三周期后nivo+ipi治疗)的结果。今年ASCO会议介绍了C组:FLOT+纳武利尤单抗(nivo)q2w一线治疗进展期或转移性胃或胃食道交界部癌的结果。主要终点是6个月时的无进展生存期,次要终点是安全性,OS和客观缓解率(ORR)。结果:纳入52名患者,65%是胃食道交界部癌。65%的患者PD-L1CPS≥1。接受FLOT和nivo的中位数为8个周期,42%接受了进一步的治疗。FLOT+nivo耐受性良好且可行,最常见的3级不良事件是中性粒细胞减少(40.4%),贫血(5.8%)和血栓栓塞事件(7.7%)。中位随访9.4个月后,3个月和6个月无进展生存率分别为85%和42%。中位PFS为6.6个月,中位OS为10.8个月。ORR和疾病控制率(DCR)分别为54%和87%。与使用mFOLFOX加nivo和ipilimumab(非随机比较)的汇总研究队列A和A1(n=90分)相比,FLOT加nivo有更高的DCR(87%比78%)和3个月PFS率(85%比72%)。结论:FLOT+nivo似乎与治疗早期疾病控制的改善有关。FLOT+nivo是侵袭性,快速进展性疾病患者的一种潜在选择。晚期后线Poster 4034 EPCAMCAR-T(IMC001)用于治疗晚期胃癌和结直肠癌IMC001是一种针对EpCAM的CAR-T细胞,在临床前研究中显示出有前景的抗肿瘤活性。方法:这项首次人体开放标签试验涉及两项单独的单位点试验。两者都遵循经典的3+3设计,剂量梯度为30、100或300万CAR-T细胞/kg。CT03是IMC001单药治疗胃癌的试验(1期),CT04包括1期和联合射频消融或微波消融治疗消化道肿瘤的2期试验。入组的是EpCAM阳性(超过10%),没有标准治疗的患者。评估IMC001的安全性、PK/PD特征和初步疗效。结果:截至2023年1月30日,有6名结直肠癌和6名胃癌的患者入选,其中一半接受了30万个细胞,另一半接受了100万个细胞/kgIMC001输注。在输注后的4周随访中,没有患者出现DLT。所有患者均出现3级血液学毒性。低剂量组中有一名患者患有免疫性肝炎SAE(3级),这可能与细胞治疗有关,发生在CAR-T输注后约11天,延长了患者的住院时间。未观察到可管理CRS(1-3级)和免疫效应细胞相关神经毒性综合征。其他与细胞治疗相关的不良事件包括CTCAE1-2级恶心、呕吐、乏力或瘙痒,这些不良事件恢复得很快。对外周血中CAR-T细胞的分析显示,所有患者的移植都很牢固,输注后第5-7天达到CAR+细胞的峰值。细胞输注后,CTC在检测极限下保持了40多周。初步疗效数据显示,在低剂量和中剂量(CT03)下,6名晚期癌症患者中有2名患者被评定为PR,3名患者仍为SD。第一位PR患者在第50周接受了第二次IMC001输注,并存活了60多周。第二例PR患者在IMC001输注后28周成功进行了胃切除手术。CT04试验正在进行中。结论:这是第一项针对EpCAM的CAR-T疗法,IMC001在晚期EpCAM+消化道肿瘤尤其是胃癌患者中显示出良好的安全性和一定的抗肿瘤活性。Poster 4052 端粒酶(OBP-301)联合帕博利珠单抗治疗胃食管腺癌的II期研究OBP-301是一种包含端粒酶基因的限制增殖性腺病毒,它与人端粒酶逆转录酶基因(hTERT)启动子结合,该基因在肿瘤中高表达,但在正常分化的成年细胞中不表达,以调节早期腺病毒基因E1A和E1B的表达。方法:符合条件的晚期胃食管腺癌患者,每两周x4次直接肿瘤注射OBP-301以及每3周静脉注射帕博利珠单抗。主要终点是ORR。采用Simon两阶段设计,要求在第一阶段的18名患者中有3个或更多的反应才能进入第二阶段。在成功完成Simon的两阶段设计中的第一阶段后,该研究关闭。结果:从2019年5月到2022年10月,招募了16名患者,中位年龄65岁(范围43-81岁),男性n=13。OBP-301直接肿瘤注射耐受性良好,中位OBP-301注射3次(范围1-5)。OBP-301的毒性包括2级疲劳/虚弱(25%)、2级发烧(18.7%),以及2级恶心、贫血、3级黑便和4级糖尿病各(6.25%)。3名患者(19%)出现部分反应(PR),从而达到Simon两阶段阈值。两名PR患者目前没有疾病证据(一名患者完成了2年的pembrolizumab治疗,一名患者在15个月后接受了原发性肿瘤切除术),第三名患者目前处于治疗的第12个月。此外,一名脑转移患者在单独进行免疫治疗后,转移性疾病消退。结论:将OBP-301病毒颗粒注射入肿瘤是可行和安全的。OBP-301与pembrolizumab在GEA中具有令人鼓舞的活性,在免疫治疗难治性疾病中具有持久的反应和活性。OBP-301+帕博利珠单抗治疗IO难治性胃食管腺癌患者的II期研究正在进行中。Poster 4043 雷莫西尤单抗联合化疗治疗Moonlight研究中FOLFOX+nivolumab+ipilimumab治疗后进展患者的疗效回顾性分析多中心随机II期AIO-STO-0417试验中一线FOLFOX+nivolumab+ipilimumab治疗后进展的的患者二线治疗的资料。患者分为两组:雷莫西尤单抗加化疗(Ram组)或单独化疗(对照组)。共纳入83例患者(雷莫西尤单抗组38例,对照组45例)。总体人群中,Ram组的PFS长于对照组(4.5个月对2.9个月)。其中,一线治疗疗效达CR/PR的39例患者中,Ram组(n=15)和对照组(n=24)二线治疗的OS分别为(9.6vs.7.5m)、PFS(5.6vs.2.9m)和DCR(53%vs.29%)。 PD-L1CPS≥1患者中,Ram组(n=16)和对照组(n=20)的OS分别为6.5vs.3.9m;PFS4.5vs.1.6m;ORR25%vs.10%,DCR44%vs.30%。结论:雷莫西尤单抗单抗作为一线FOLFOX加双检查点抑制治疗进展后的二线治疗是有效的,尤其是对有初始反应和PD-L1阳性表达的患者。Poster 4035 CLDN18.2在局部晚期无法切除或转移的胃或胃食道交界处腺癌患者中的全球流行率:两项佐妥昔单抗3期研究的生物标记物分析(SPOTLIGN和GLOW)SPOTLIGHT和GLOW3期研究表明,在CLDN18.2+/HER2-胃或胃食道交界处腺癌患者中,使用CLDN18.2靶向抗佐妥昔单抗+化疗能够延长患者的PFS和OS。会议上研究者报道了两项研究中生物标志物分析结果。在SPOTLIGHT和GLOW中,3576例患者的CLDN18IHC结果有效;CLDN18.2+肿瘤1399例(39.1%)。CLDN18.2在女性患者中的阳性率为43.7%(513/1175),在男性患者中为36.9%(886/2401)。欧洲/中东地区的CLDN18.2阳性率为44.0%(671/1524),北美地区为37.7%(183/485),亚太地区为36.5%(479/1314)。胃癌患者CLDN18.2的阳性率为41.0%(1056/2576),GEJ腺癌患者为37.3%(302/809)。CLDN18.2在弥漫性疾病患者中的阳性率(48.9%,479/980)高于肠型胃癌患者(38.9%,265/682)。在从转移部位收集的肿瘤中,CLDN18.2的患病率为41.1%(175/426),在从原发部位收集的瘤中为38.6%(1195/3094)。结论:SPOTLIGHT和GLOW3期研究是迄今为止确定全球CLDN18.2流行率的最大数据来源。CLDN18.2在约35-40%的不可切除或mG/GEJ腺癌患者中具有高肿瘤表达。
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科29人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科29人已读 - 胃癌前沿进展 2023 ASCO-GI 胃癌相关研究
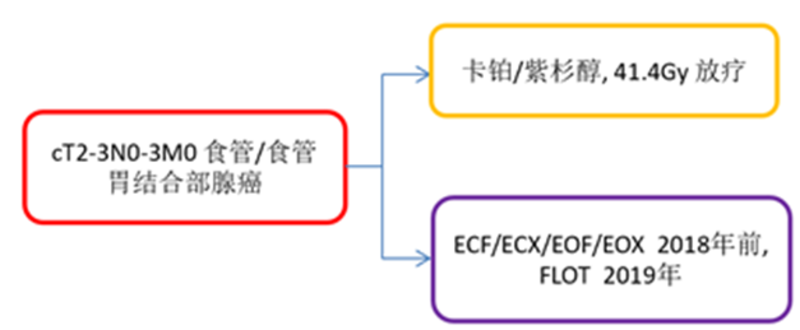
今年的ASCOGI大会于当地时间2023年1月19日至21日在旧金山召开。分享几篇关于胃癌/食管胃结合部癌药物治疗的摘要。新辅助治疗RapidAbstract295:NEO-AEGIS研究最终结果初步分析Neo-Aegis是比较同步放化疗(CROSS方案:卡铂/紫杉醇+41.4Gy放疗)与围术期MAGIC/FLOT化疗治疗食管胃结合部腺癌的III期临床研究。研究设计主要研究终点:总生存结果:377例cT2-3N0-3M0食管胃结合部腺癌患者随机分组为围手术期化疗组(184例)或CROSS治疗组(178例)。初始样本量计算是基于CROSS组疗效优于围手术期化疗10%。在第一次无效性分析后,主要研究终点被修改为围手术期化疗的疗效不劣于同步放化疗。2021ASCO报道了该研究第二次无效性分析的结果,共有143例死亡,新辅助放化疗组70例,新辅助化疗组73例,估计3年生存率分别为56%和57%。基于此数据,数据和安全监察委员会建议结束招募。今年的ASCO-GI上报道了中位随访34.2(0.43-111.8)个月的结果,共有186人死亡,CROSS组91人,围手术期化疗组95人,估计的3年生存率分别为57%和55%,HR1.03(95%可信区间0.77-1.38)。食管胃结合部癌泛指发生于食管胃解剖交界线上下约5cm范围内的腺癌。食管胃结合部癌的最佳综合治疗模式尚不明确。FLOT4-AIO研究中有56%患者为食管胃结合部癌,提示食管胃结合部癌患者围手术期化疗是一种有效治疗方法。CROSS研究结果显示新辅助放化疗+手术与单纯手术相比提高了食管胃结合部癌患者的生存。对于食管胃结合部癌,新辅助放化疗与围手术期化疗两种治疗模式的疗效是否有差异?与POET研究目的类似,Neo-AEGIS研究旨在比较新辅助放化疗与围手术期化疗治疗食管胃结合部癌的疗效。此次生存结果与既往报道一致,围手术期化疗在生存上不劣于术前放化疗,但在R0切除率和pCR率方面,同步放化疗优于围手术期化疗。Poster354JCOG1704研究:多西紫杉醇、奥沙利铂和S-1联合D2胃切除加腹主动脉旁淋巴结清扫术治疗有广泛淋巴结转移胃癌的II期研究方法:研究纳入的是初治的胃腺癌,胃主要分支动脉周围肿大结节(肿大N)和/或腹主动脉旁转移(PAN);cM0(主动脉旁结节除外);灌洗液细胞学阴性。术前多西紫杉醇、奥沙利铂联合S-1化疗3周期,然后行D2+腹主动脉旁淋巴结清扫术。术后采用S-1辅助化疗1年。主要终点是主要病理缓解率(肿瘤消退超过三分之二)。主要病理反应率的期望值和阈值分别设定为40%和25%。结果:共纳入47例患者,符合疗效分析的46位患者中,20例仅有块状N,17例仅有PAN,10例同时有块状N和PAN。临床分期:III期19例,IV期28例。46例完成了术前DOS。行胃切除术44例(94%),其中远端胃切除23例,全胃切除21例,R0切除43例(91%)。46例患者中,26例(57%)有明显病理反应,其中pCR24%。按Becker分级标准,3级13例,2级12例,1b级7例,1a级11例。与手术相关的3/4级毒性反应为腹壁脓肿5例(12%),胰瘘3例(7%)。没有观察到与治疗相关的死亡。目前,PAN转移在TNM分期中被归为M1期,视为远处转移,不包括在标准的D2淋巴结清扫范围内。但也有研究者建议考虑将胃癌转移至PAN视为可切除的病例而不是转移性肿瘤,因为与其他转移性胃癌相比,在此类患者中观察到的长期结局要好得多。JCOG0001、JCOG0405和JCOG1002三项研究均是针对腹主动脉旁淋巴结转移的胃癌患者,术前新辅助化疗联合腹主动脉旁淋巴清扫的Ⅱ期临床试验,结果表明术前化疗然后行D2+腹主动脉旁淋巴结清扫术可以改善患者生存。JCOG1704研究也提示胃癌术前DOS+D2+腹主动脉旁结节清扫术是一种安全、可行的治疗胃癌合并广泛淋巴结转移的方法。辅助Poster308化疗在临床T2N0M0胃癌中的作用对于病理分期I期的胃癌患者是否可以从术后辅助化疗中获益尚不明确。研究回顾性分析了2006至2017年美国国家肿瘤数据库中术后分期为T2N0M0的3142名胃腺癌患者。将这些患者分为3组:单纯手术组(S)2,090例(66.5%)、手术后辅助化疗组(AC)360例(11.5%)和围手术期化疗组(POC)692例(22.0%)。采用单变量和多变量COX比例风险模型评价总生存率的差异。根据检查的区域淋巴结数量,患者被分为两个亚组,小于15个(RNE<15个)1526例(49.2%)和大于或等于15个(RNE≥15)1577例(50.8%)。在多变量模型中,手术后辅助性化疗(HR0.75,p=0.003)、RNE≥15(HR0.73,p=0.001)、在学术机构接受治疗(HR0.84,p=0.005)、女性(HR0.84,p=0.004)和亚裔(HR0.69,p=0.002)的患者有更好的结果。亚组分析显示,围手术期化疗对RNE<15有利(HR0.74,p=0.029)。在多变量模型中,RNE≥15的患者,接受手术后辅助性化疗(HR0.72,p=0.017)的存活率有所提高。结论:对于T2N0M0期胃癌患者,手术后辅以化疗是有益的。Poster386Ⅲ期胃腺癌根治性D2切除术后辅助nab-紫杉醇+S-1治疗的III期临床研究研究旨在评价nab-紫杉醇联合S-1(AS)和奥沙利铂联合卡培他滨(CAPOX)治疗D2根治性胃切除术后III期胃腺癌(GAC)的疗效和安全性。方法:本研究为3期开放随机研究,入组的是D2根治性胃切除术后病理分期为III期的胃癌患者。随机分为AS组(nab-紫杉醇100mg/m2,第1、8天;S-140~60mg,每日2次,第1~14天)或CAPOX,每3周重复,共8个周期。主要终点是意向治疗分析的3年无病生存率(DFS)。次要终点包括总体存活率(OS)和安全性。结果:在2020年3月至2022年8月期间,233名患者被随机分配到研究治疗(AS,115例;CAPOX,118例)。AS的病理分期为IIIA期42.61%,IIIB期34.78%,IIIC期22.61%;CAPOX病理分期IIIA期47.46%,IIIB期30.51%,IIIC期22.03%。AS组1年DFS率为89.0%,CAPOX组为76.9%。AS组的1年OS率高于CAPOX组(100%比95.5%)。AS组复发7例(6.09%),CAPOX组复发11例(9.32%)。AS和CAPOX的复发部位涉及腹膜(1vs4)、局部复发(1vs2)和远处复发(5vs6)。AS(38.26%)和CAPOX(22.03%)患者出现3/4级不良事件(AEs)。AS和CAPOX最常见的不良反应包括贫血(20.96%vs19.63%)、中性粒细胞减少症(30.70%vs21.02%)和血小板减少症(1.10%vs15.47%)。结论:在这项研究中,AS显示了与CAPOX相比,根治性D2胃切除后III期GAC患者的DFS率、OS率有更长的趋势,有待于更长时间随访结果。晚期一线(化疗)Poster380晚期胃癌转化治疗前瞻性多中心II期研究CCOG1403的长期生存结果方法:研究纳入的是初诊不可切除治愈的胃癌患者,1个疗程以上化疗后,行诊断性腹腔镜术或开腹手术。对于可治愈的病例行胃切除术。主要终点是从一线化疗开始算起的3年生存率。结果:从2014年4月至2019年3月,共纳入30名患者。不可治愈因素包括淋巴结转移,腹膜转移,肝转移等。Yoshida’s的分类:I类3例,II类16例,III类8例,IV类2例。化疗方案包括SOX(11例)、SP(8例)、XP+HER(8例)、PTX腹腔灌注方案(6例)和其他方案(12例)。术前化疗疗效评价:PR24例,SD6例。手术方式:全胃切除(18例)、远端胃切除(7例)、近端胃切除(1例)。80%(24例)获得R0切除。病理结果显示26.7%(8/30)的患者出现主要反应。在30例患者中,66.3%的患者一线化疗后存活3年以上。胃癌的转化治疗是针对初始部分不可切除,但有潜在手术切除机会的胃癌患者,接受全身系统化疗后,其不可切除因素出现部分或完全缓解,行R0切除,从而获得相对较长的术后生存时间和(或)无复发生存时间。目前初始不可切除胃癌转化治疗尚处于探索阶段,相关研究主要为一些单中心、小样本、回顾性的报道。CCOG1403是小样本前瞻性研究,对于初始不可手术的胃癌患者,经过转化治疗,3年生存率达到66.3%,有待开展随机试验进行验证。Poster313进展期胃食管腺癌一线两药化疗与三药化疗的真实世界研究方法:研究分析了美国一电子健康记录(EHR)数据库,比较在一线两药化疗和三药化疗的疗效。研究回顾2011至2022年间接受一线细胞毒性两药或三药治疗的胃及食管胃结合部癌(AGEA)患者。使用KaplanMeier和Cox比例风险模型比较两组间的生存结果。结果:5375例符合纳入标准的AGEA患者中,4415例(82%)接受了两药化疗,960例(17%)接受了三药化疗。接受两药化疗患者的中位OS为11个月,与接受三药化疗患者的中位OS(11个月,95%可信区间10-12)相似。控制了性别、种族、吸烟状况、发病地点以及HER2和PD-L1状态等潜在混杂变量的Cox比例风险模型显示,两组的预后没有显著差异(HR0.9,95%CI0.8-1)。亚组分析比较FLOT和FOLFOX/CapeOx方案疗效显示,FLOT的mOS改善优于FOLFOX/CapeOx方案(13mvs10m)。多变量分析中得到一致的结果,与FLOT相比,FOLFOX/CapeOX的死亡风险增加(HR1.2,95%CI1-1.4)。结论:与既往研究一致,这项真实世界的研究没有发现在AGEA中一线使用三药化疗与两药化疗的生存差异。然而,当将分析局限于现代化疗方案时,结果表明,与FOFOX/CapeOX相比,使用FLOT可能存在生存益处。晚期一线(免疫)·GeneralSession286Rationale305:替雷利珠联合化疗一线治疗进展期胃或食管胃交界部腺癌的III期临床研究研究设计结果:546名PD-L1+患者中,274名患者随机接受替雷利珠联合化疗,272名患者接受安慰剂+化疗治疗。替雷利珠单抗+化疗显示出具有统计学意义和临床意义的OS改善(HR0.74[95%CI:0.59-0.94],mOS17.2vs12.6个月;单侧P=0.056)。与安慰剂+化疗相比,替雷利珠单抗+化疗的PFS也更长(mPFS7.2vs5.9个月;HR0.67[95%CI=0.55-0.83]),ORR更高(50.4%vs43.0%),反应更持久(mDoR9.0vs7.1个月)。结论:在RATIONALE305中,替雷利珠+化疗与安慰剂+化疗相比,在OS方面有显著且有临床意义的改善。·OralAbstract325CheckMate649研究的3年随访结果CheckMate649研究是评估NIVO+化疗一线治疗晚期胃癌/食管胃交界处癌/食管腺癌的III期临床研究。此次会议报道了CheckMate649的3年随访结果。结果:581例患者同时随机接受NIVO+化疗或化疗。在至少36个月的随访中,NIVO+化疗继续显示PD-L1CPS≥5患者和所有随机患者的OS和PFS优于化疗。PD-L1CPS≥5患者在基线时有可测量病变的客观有效率NIVO+化疗组为60%,化疗组为45%。在所有随机患者中,NIVO+化疗组的ORR为58%(95%CI54–62),化疗组为46%(95%CI42–50)。在PD-L1CPS≥5的患者中,NIVO+化疗组比化疗组的反应更持久,反应中位持续时间分别胃9.6个月vs7.0个月,在所有随机患者中(mDOR]8.5个月[9%可信区间7.7-9.9]vs6.9个月[995%可信区间5.8-7.2])。在大多数预先指定的亚组中观察到NIVO+化疗对OS的益处。结论:经过3年的随访,NIVO+化疗继续显示出具有临床意义的长期生存益处,具有可接受的安全性,进一步支持其作为先前未经治疗的晚期GC/GEQC/EAC患者的标准1L治疗。晚期一线(靶向)·OralAbstractLBA292Spotlight研究:佐妥昔单抗+mFOLFOX6一线治疗CLDN18.2+/HER2-局部晚期无法切除或转移性胃或胃食道交界处腺癌的3期研究方法:初治CLDN18.2+/HER2-不可切除局部晚期或转移性胃或胃食管交界处腺癌患者1:1随机分为佐妥昔单抗+mFOLFOX6或安慰剂+mFOLVOX6。主要终点为PFS。次要终点包括OS、ORR和安全性。结果:565名患者被1:1随机分为佐妥昔单抗+mFOLFOX6(N=283)或安慰剂+mFORFOX6组(N=282)。佐妥昔单抗+mFOLFOX6显著改善PFS(中位数10.61vs8.67个月,HR0.751,P=0.0066)和OS(中位数18.23vs15.54个月,HR0.750,P=0.0053,)。两组ORR分别为53.8%vs48.8%。佐妥昔单抗+mFOLFOX6最常见的TEAE为恶心(佐妥昔单抗组与安慰剂组分别为82.4%与60.8%)、呕吐(67.4%与35.6%)和食欲下降(47.0%与33.5%);结论:佐妥昔单抗+mFOLFOX6显著延长CLDN18.2+/HER2-局部晚期无法切除或转移性胃或胃食道交界处腺癌患者的PFS和OS。Poster347泽尼达妥单抗+化疗一线治疗HER-2阳性转移性胃食管腺癌的II期临床研究方法:入组的是晚期初治Her-2阳性胃食管腺癌患者,给予泽尼达妥单抗(一种针对ECD4和ECD2的抗HER2双特异性抗体)+化疗的治疗(mFOLFOX6、CAPOX或FP)。结果:46名接受泽尼达妥单抗+化疗治疗的患者中位随访时间为21.5个月,20名患者(43%)仍在接受治疗。确认的客观缓解率(cORR)为79%,疾病控制率为92%;3名患者获得完全缓解。在所有42例患者中,中位无进展生存期(PFS)为12.5个月,中位总生存期(OS)尚未达到。18个月的生存率估计为87.3%。所有患者中最常见的治疗相关不良事件是腹泻、恶心、周围感觉神经病变、食欲下降、疲劳、呕吐和低钾血症。结论:对于HER2阳性晚期食管胃腺癌患者,泽尼达妥单抗+化疗是一种高度有效的治疗方案,具有可控的安全性。Toga研究确立了曲妥珠单抗+化疗一线治疗Her-2阳性胃癌的地位,研究显示,曲妥珠单抗组的中位PFS为6.7个月,中位总生存期为13.8个月,客观有效率达到47.8%。此II期研究结果显示泽尼达妥单抗+化疗有更好的PFS,OS和客观有效率。期待III期研究的结果。晚期二线及以后OralAbstract289HERIZON:HER2靶向多肽疫苗HER-Vaxx(IMU-131)联合标准化疗治疗HER2过表达的转移性或晚期胃/食管胃结合部腺癌患者的Ⅱ期研究研究设计结果:在36例随机分组的患者中(19例接受HER-Vaxx联合化疗,17例单独化疗),32例患者在最终分析时出现生存事件(分别为15例和17例)。所有患者均接受奥沙利铂+卡培他滨化疗。与单纯化疗相比,HERVaxx联合化疗的患者存活获益为42%。这转化为HR为0.580(80%双侧CI:0.362,0.927),p值为0.066,有统计学意义。接受HERVaxx联合化疗的患者的中位OS为14.0个月,而仅接受化疗的患者为8.3个月。HERVaxx组的中位反应持续时间为30周,单纯化疗组为19周。两个治疗组的安全性没有差异。结论:这些数据表明,在HER2过度表达的胃/食管胃结合部癌症患者中,HER2主动免疫HERVaxx是安全的,并提供了超过标准化疗的临床益处。Poster342应用JCOG1013的资料研究进展期胃癌的预后指标研究者既往报告过,PS评分≥1,未行胃切除术,转移部位数量≥2,和血清ALP水平高是进展期胃癌不良预后因素,并通过分析JCOG9912研究中的晚期胃癌患者的数据,提出了JCOG预后指数。方法:使用Cox比例回归模型,回顾性分析预后因素对JCOG1013研究中纳入的的进展期胃癌患者生存的预测价值。结果:在741名患者中,选择了730名具有本分析所需数据的患者。根据既往JCOG指数,将患者分为良好(n=233)、中等(n=444)和较差(n=53)风险组,三组的中位OS分别为19.0、14.2和9.1个月。与良好组相比,中等组的HR为1.59[95%CI,1.33–1.89;p<0.0001],差组为2.47[95%CI;1.81–3.38;p<0.001]。在7个因素的多变量分析中,单变量分析显示:PS≥1,弥漫型,转移部位数量≥2,NLR(中性粒细胞/淋巴细胞数比值)≥3.1与预后差显著相关,而之前没有胃切除、腹膜转移和血清ALP水平高则无相关性。根据四个新确定的预后危险因素提出改良JCOG预后指数。基于改良JCOG预后指数,患者被分为三组:良好(无危险因素)、中等(1或2)和较差(3或4)三组。良好(n=221)、中等(n=441)和较差(n=68)风险组的中位OS分别为20.6、13.7和9.4个月。与良好组相比,中等组的HR为1.70[95%CI,1.42–2.03;p<0.0001],差组为3.11[95%CI;2.33–4.14;p<0.001]。结论:改良的JCOG预后指数可以将JCOG1013研究中患者的OS明显分层。
 蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科92人已读
蒲汪旸 主任医师 苏州大学附属第二医院 肿瘤科92人已读





